Termodynamika
Kalorimetrická rovnica
$\triangle{}t_1c_1m_1 = \triangle{}t_2c_2m_2$
# 0-tý zákon
Ak sú systémy A a B v rovnováhe so systémom T (teplomerom), tak budú v rovnováhe navzájom a priradzujeme im rovnakú teplotu.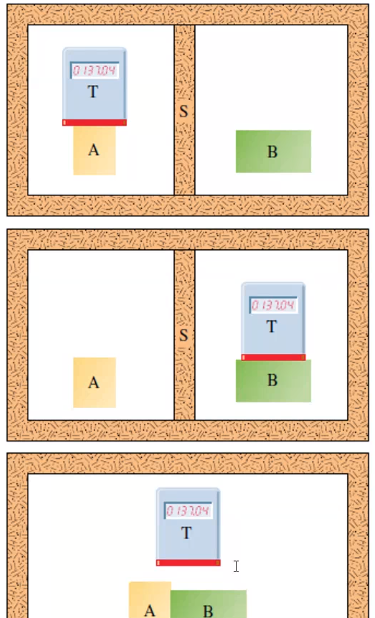
# 1. Zákon
Q = 0 - adiabatický jav
$Q=\Delta U + \Delta W$
$\Delta U = m*c*\Delta T$
Zmena vnútornej energie môže nastať:
- konaním práce
- prenosom tepla
Kruhový dej:
- konečný a začiatočný stav je totožný
- graf vyjadrujúci tlak p funkciou objemu V tvorí uzavretú krivku
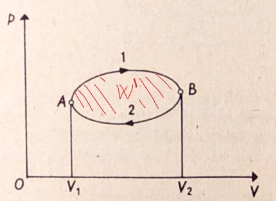
- plocha uzavretej krivky je W’ = práca plynu = $p*\Delta V$
aka. $\int_{p_1}^{p_2}{V\ dp} = \int_{p_1}^{p_2}{\frac{nRT}{p}\ dp}$
$\quad = nRT*(ln(p_2)-ln(p_1))$
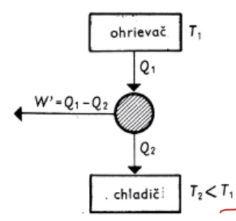
# 2. Zákon
Nie je možné zostrojiť periodicky pracujúci tepelný stroj, ktorý by teplo od
istého telesa (ohrievača) iba prijímal a vykonával rovnako veľkú prácu.